Menschliche Faktoren und Benutzerfreundlichkeitstests für Medizinprodukte
Warum sich Unternehmen für NAMSA entscheiden
Medtech-Unternehmen werden mit maßgeschneiderten Forschungsprojekten unterstützt
Abgeschlossene Projekte zur Benutzerfreundlichkeit von Medizinprodukten
Mitarbeiter mit klinischen und regulatorischen Spezialisten für Medizinprodukte
Panel aus HCP- und Administrator-Teilnehmern in unserer globalen Datenbank
Die Bedeutung von Humanfaktoren und Usability-Tests bei der Entwicklung medizinischer Geräte
Menschliche Faktoren spielen eine entscheidende Rolle bei der Entwicklung von Medizinprodukten und gewährleisten, dass diese nicht nur funktional, sondern auch intuitiv und benutzerfreundlich sind. Durch die Integration menschlicher Faktoren von der frühen Designphase bis hin zu Anpassungen nach der Markteinführung können Hersteller Geräte entwickeln, die den Bedürfnissen der Endnutzer entsprechen, die Sicherheit erhöhen und die Gesamteffektivität verbessern. Dieser nutzerzentrierte Ansatz trägt dazu bei:
- Optimierung der Produktkonzeptentwicklung
- Potenzielle Usability-Probleme identifizieren und beheben
- Einhaltung gesetzlicher Bestimmungen und Genehmigung
- Liefern Sie Produkte, die sowohl innovativ als auch zuverlässig sind.
Diese Forschung trägt direkt zur Verbesserung des Gerätedesigns, der Benutzerschulung und der klinischen Protokolle bei. Bei sorgfältig durchgeführten Tests können Hersteller 97 % der Usability-Probleme identifizieren.
Wir bei NAMSA verstehen die entscheidende Bedeutung menschlicher Faktoren und engagieren uns dafür, Sie bei der Entwicklung und Prüfung von Medizinprodukten zu unterstützen, die wirklich etwas bewirken.
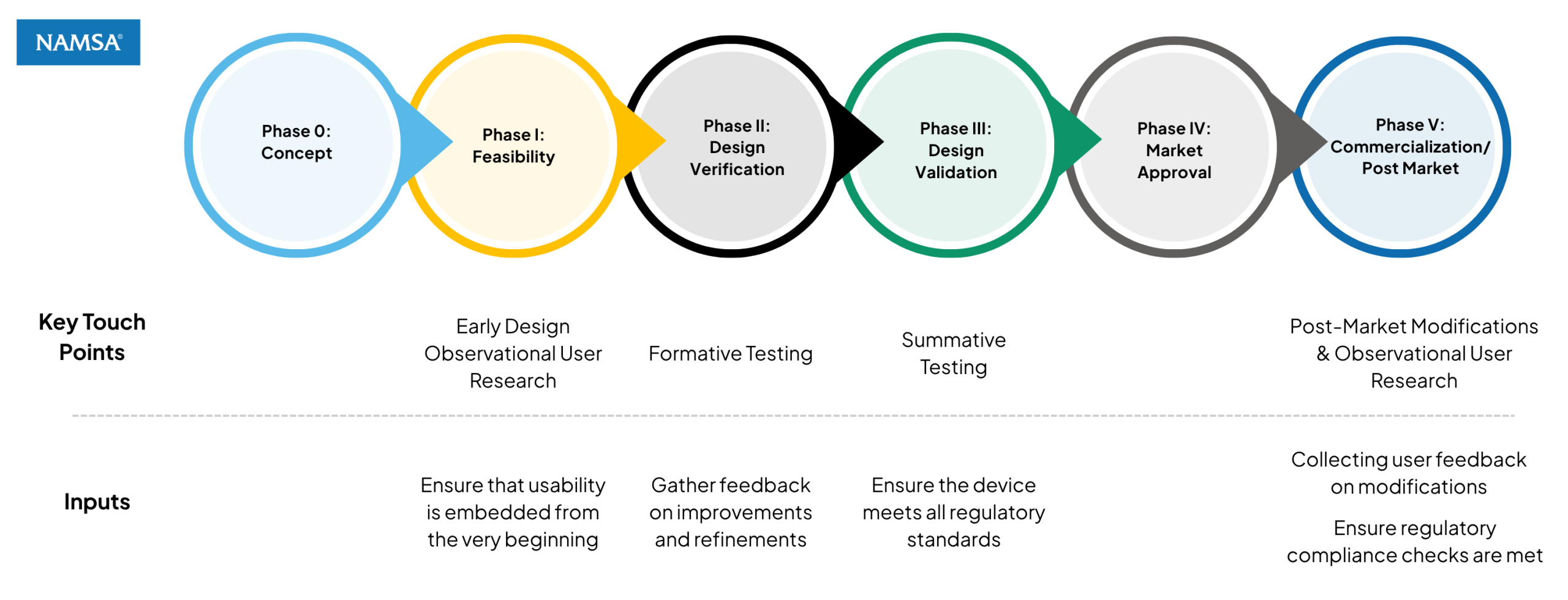
Wichtige Berührungspunkte bei Human Factors und Usability-Tests
Um umfassende Benutzerfreundlichkeit und die Einhaltung gesetzlicher Vorschriften zu gewährleisten, können menschliche Faktoren in verschiedenen Phasen des Produktlebenszyklus integriert werden. Die wichtigsten Berührungspunkte, an denen dies geschieht, sind: NAMSA kann Sie bei Ihren Tests zu menschlichen Faktoren unterstützen:
- Frühe Entwurfsphase: Zu Beginn arbeiten unsere Experten für Mensch-Maschine-Interaktion eng mit Geräteentwicklern und Designern für Mensch-Maschine-Interaktion zusammen. In dieser Phase werden erste Produktkonzepte, Wireframes und Designskizzen erarbeitet, um die Benutzerfreundlichkeit von Anfang an zu gewährleisten.
- Prototypenentwicklung: Im weiteren Verlauf werden formative Testphasen mit Ingenieuren und potenziellen Nutzern durchgeführt. In dieser Phase sammeln wir wertvolles Nutzerfeedback zu Prototypen, Modellgeräten und virtuellen Formaten, was iterative Verbesserungen und Optimierungen ermöglicht.
- Marktzulassung: Kurz vor der Fertigstellung des Produkts werden abschließende Tests mit den finalen Endnutzergruppen durchgeführt. Diese strenge Phase umfasst formale Usability-Testprotokolle, Videoaufnahmen aus verschiedenen Blickwinkeln und detaillierte Beobachtungen, um sicherzustellen, dass das Gerät alle regulatorischen Standards erfüllt.
- Regulatorische Standards:
- Anwendung von Human Factors und Usability Engineering auf Medizinprodukte: FDA-Leitfaden (2016)
- IEC 62366-1: Usability Engineering für Medizinprodukte
- IEC 14971: Anwendung des Risikomanagements auf Medizinprodukte
- Änderungen nach der Markteinführung: Auch nach der Markteinführung eines Produkts bleiben menschliche Faktoren entscheidend. Wir führen Tests für Geräte-Upgrades oder Änderungen der Produktversprechen durch, sammeln Nutzerfeedback zu den Änderungen, werten Usability-Testergebnisse aus und stellen die Einhaltung gesetzlicher Bestimmungen sicher.
Geh den nächsten Schritt
Möchten Sie mehr über unsere Erfahrung im Bereich Human Factors und Usability erfahren?
Regulatorische Anforderungen an Usability-Tests
Die Prüfung der Benutzerfreundlichkeit und der Anwenderfaktoren ist unerlässlich, um die Sicherheit und Wirksamkeit von Medizinprodukten für die vorgesehenen Anwender, Anwendungsbereiche und Umgebungen zu gewährleisten. Die US-amerikanische Arzneimittelbehörde FDA schreibt diese Studien vor, insbesondere für Hochrisikoprodukte, bei denen Anwendungsfehler erhebliche Schäden verursachen können. Die FDA-Richtlinien unterstreichen die Bedeutung von Validierungsstudien zur Benutzerfreundlichkeit als Teil des Zulassungsverfahrens vor dem Inverkehrbringen. Daher ist die Anwendungsprüfung ein entscheidender Schritt für Hersteller, die neue Produkte auf den Markt bringen wollen.
Über die FDA-Anforderungen hinaus müssen Hersteller von Medizinprodukten auch weitere regionale Vorschriften einhalten, wie beispielsweise die Medizinprodukteverordnung (MDR) und die Verordnung über In-vitro-Diagnostika (IVDR) der Europäischen Union sowie die australische Arzneimittelbehörde (TGA). Diese Vorschriften betonen gleichermaßen die Bedeutung von Anwendungstests, um die Sicherheit und Wirksamkeit der Produkte zu gewährleisten, und erfordern umfassende Studien zu menschlichen Faktoren während des gesamten Produktlebenszyklus.
Bei NAMSA unterstützen wir die Einhaltung aller Vorschriften, da wir internationale Standards befolgen und Experten für die Details und Feinheiten globaler regulatorischer Anforderungen im Bereich der menschlichen Faktoren sind. Unser Team stellt sicher, dass Ihre Geräte alle notwendigen Richtlinien erfüllen, was einen reibungslosen Markteintritt ermöglicht und höchste Standards in puncto Sicherheit und Benutzerfreundlichkeit gewährleistet.
Vertrauen können NAMSA um Ihre Tests zum menschlichen Faktor durchzuführen
Wir bei NAMSA sind stolz darauf, herausragende Dienstleistungen im Bereich Human Factors und Usability-Tests für Medizinprodukte anzubieten. Unser einzigartiges Leistungsversprechen basiert auf mehreren Kernkompetenzen:
- Unsere Fähigkeit, kreative, kostengünstige und effiziente Testlösungen zu liefern, die auf Ihre spezifischen Bedürfnisse zugeschnitten sind
- Dank unseres umfangreichen Netzwerks an medizinischen Fachkräften und Patienten gewährleisten wir eine schnelle und zuverlässige Rekrutierung von Studienteilnehmern.
- Unsere profunden regulatorischen Kenntnisse garantieren, dass Ihre Produkte alle erforderlichen Konformitätsstandards erfüllen und ermöglichen so einen reibungsloseren Markteintritt.
- Unser kollaborativer Ansatz und unsere Kompetenz in der Verhaltensforschung ermöglichen es uns, aufschlussreiche Analysen und umsetzbare Empfehlungen zu liefern und so sicherzustellen, dass Ihre Geräte nicht nur konform, sondern auch intuitiv und benutzerfreundlich sind.
Mit NAMSA gewinnen Sie einen Partner, der sich der Verbesserung von Sicherheit, Wirksamkeit und Benutzerfreundlichkeit Ihrer Medizinprodukte verschrieben hat. Unser Engagement für Kreativität, regulatorische Expertise und partnerschaftliche Zusammenarbeit gewährleistet, dass Ihre Produkte nicht nur konform, sondern auch intuitiv und benutzerfreundlich sind und so das Leben der Endanwender spürbar verbessern.
Häufig gestellte Fragen (FAQs)
Welchen Umfang an Tests zur Ergonomie erwartet die FDA für unser Gerät?
Die Erwartungen der FDA hängen vom Risikoprofil Ihres Produkts, den vorgesehenen Anwendern und der Einsatzumgebung ab. NAMSA Die Prüfstelle überprüft in der Regel Ihre anwendungsbezogene Risikoanalyse, die Geräteklassifizierung und alle bisherigen Arbeiten im Bereich Herzinsuffizienz, um festzustellen, ob formative Studien, eine vollständige Validierungsstudie oder zusätzliche Begründungen erforderlich sind. Außerdem wird beurteilt, ob Ihr Gerät unter die FDA-Richtlinien für „kritische Aufgaben“ fällt, was den Umfang der Prüfungen bestimmt. Ziel ist es, sicherzustellen, dass Ihr Herzinsuffizienzprogramm den FDA-Richtlinien entspricht und Überraschungen während der Prüfung vermieden werden.
Wie funktioniert NAMSA Die geeigneten Benutzergruppen, Umgebungen und kritischen Aufgaben ermitteln?
NAMSA Wir analysieren die vorgesehenen Nutzer, Anwendungsgebiete und das Risikoprofil Ihres Geräts, um repräsentative Nutzergruppen und realistische Einsatzumgebungen zu definieren. Wir überprüfen Ihre Risikoanalyse, Kennzeichnung und Arbeitsabläufe, um Aufgaben zu identifizieren, die bei fehlerhafter Ausführung zu Schäden führen können. Diese werden zu „kritischen Aufgaben“, die in einer Validierungsstudie evaluiert werden müssen. NAMSA Berücksichtigt werden auch Grenzfälle – wie beispielsweise Nutzer mit geringen Lese- und Schreibfähigkeiten oder stressige Umgebungen –, um sicherzustellen, dass die Studie die reale Anwendung widerspiegelt und den Erwartungen der FDA hinsichtlich Diversität und Realismus entspricht.
Welche Stichprobengröße und Rekrutierungsstrategie erfüllen die Anforderungen der FDA?
Die Stichprobengröße richtet sich nach den Erwartungen der FDA an eine aussagekräftige Repräsentation jeder Nutzergruppe und nicht nach der statistischen Aussagekraft. NAMSA Für Validierungsstudien werden üblicherweise mindestens 15 (+1 Pilot-)Teilnehmer pro Nutzergruppe empfohlen, abhängig von der Gerätekomplexität und dem Risiko. Bei der Rekrutierung liegt der Fokus darauf, Teilnehmer zu finden, die hinsichtlich Erfahrung, demografischer Merkmale und Schulungsniveau den Zielnutzern entsprechen. NAMSA Zudem wird sichergestellt, dass die Teilnehmer mit dem Gerät nicht vertraut sind, es sei denn, die Anwendung im realen Einsatz erfordert eine vorherige Schulung. Dieser Ansatz trägt dazu bei, die Anforderungen der FDA hinsichtlich Realismus und Repräsentativität der Nutzer zu erfüllen.
Wie funktioniert NAMSA Strukturierung der Dokumentation zu Human Factors gemäß den FDA-Einreichungsstandards?
NAMSA Es wird ein Bericht zur Validierung der menschlichen Faktoren erstellt, der der von der FDA empfohlenen Struktur entspricht: Gerätebeschreibung, Anwenderprofile, Anwendungsumgebungen, Risikoanalyse, Zusammenfassungen formativen Studienmaterials, Validierungsstudienprotokoll, Ergebnisse und Schlussfolgerungen. Dabei wird sichergestellt, dass die Darstellung risikobasierte Entscheidungen klar mit dem Studiendesign verknüpft und belegt, dass verbleibende anwendungsbedingte Risiken akzeptabel sind. Der Bericht enthält außerdem detaillierte Aufgabenanalysen, demografische Daten der Teilnehmer und beobachtete Anwendungsfehler. Ziel ist es, eine kohärente, evidenzbasierte Darstellung zu präsentieren, die zeigt, dass das Gerät sicher und effektiv eingesetzt werden kann.
Welcher Zeitrahmen und welche Kosten sind für Human Factors-Tests und die Berichterstattung mit NAMSA zu erwarten?
Die Zeitpläne variieren je nach Gerätekomplexität, Rekrutierungsaufwand und Anzahl der Studienrunden. Eine typische formative Studie dauert 6–10 Wochen, während eine vollständige Validierungsstudie – einschließlich Protokollentwicklung, gegebenenfalls Ethikkommissionsprüfung, Rekrutierung, Testung und Berichterstattung – oft 12–20 Wochen in Anspruch nimmt. Die Kosten hängen von der Teilnehmerzahl, den Studienorten und dem erforderlichen Dokumentationsumfang ab. NAMSA bietet einen detaillierten Projektplan mit Meilensteinen, Abhängigkeiten und Budgetrahmen, damit Sie die HF-Aktivitäten mit Ihrer Strategie für die Zulassungsunterlagen abstimmen können.
Lernen Sie unsere Experten für Mensch-Computer-Interaktion und Usability-Forschung kennen
Dank unserer umfassenden Erfahrung in der Medizingerätebranche unterstützen wir Sie bei der Konzeption und Durchführung von Studien, die den gesetzlichen Standards entsprechen und in der Praxis Wirkung zeigen.
-
Adam E. Saltman, MD, PhD
 Chief Medical OfficerBiografie anzeigen
Chief Medical OfficerBiografie anzeigen -
Monica R. Montañez, MS, RAC, CQA
 Leitender Strategieberater, RegulierungBiografie anzeigen
Leitender Strategieberater, RegulierungBiografie anzeigen -
Matt Royle, PhD
 Leitender RegulierungsberaterBiografie anzeigen
Leitender RegulierungsberaterBiografie anzeigen -
David Mandley, PhD
 Leitender RegulierungsberaterBiografie anzeigen
Leitender RegulierungsberaterBiografie anzeigen -
Kevin Butcher
 Leitender RegulierungsberaterBiografie anzeigen
Leitender RegulierungsberaterBiografie anzeigen
Ähnliche Dienstleistungen, die Sie interessieren könnten

US FDA & CMS Beratung

EU MDR & IVDR Consulting